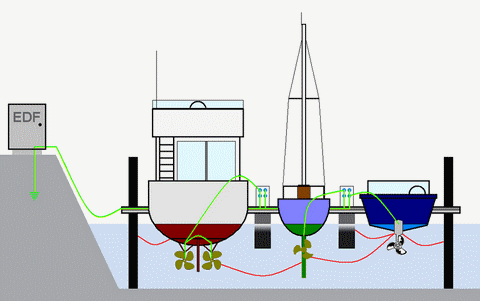
Electrolyse (& Corrosion...)
L'électrolyse
Le terme "électrolyse" se réfère ici, par abus de langage dans le milieu maritime, aux phénomènes naturels de corrosion galvanique et accidentels de corrosion électrolytique. La corrosion des métaux est un phénomène électro-chimique naturel, complexe et multiforme : elle met en jeu des courants électriques naturels et/ou indésirables détectables et affecte tant la sécurité des équipages que la valeur des bateaux atteints.
La corrosion
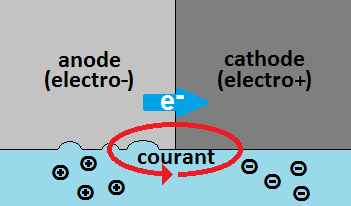
La corrosion est la conséquence d'un déplacement d'électrons (donc d'un courant électrique...), naturel et/ou accidentel, entre une surface métallique anodique (ex. vos anodes zinc) et une surface métallique cathodique (ex. votre jambe de sail-drive aluminium), reliées conductivement et immergées dans un même électrolyte (ex. l'eau de mer). Il y a destruction de matière à l'anode et protection à la cathode, d'où le terme "protection cathodique".
Galvanique vs électrolytique
La corrosion galvanique est liée aux différences naturelles de potentiel existantes entre différents métaux en contact dans un même électrolyte (eau conductrice...), à l'origine de la circulation d'un courant électrique de très faible intensité : le courant de corrosion. Elle est efficacement combattue par les anodes sacrificielles qui délivrent naturellement un courant de protection s'opposant au courant de corrosion. Attention, la protection cathodique qu'elles procurent ne se présume pas : elle se mesure !
La corrosion électrolytique, quant à elle, est provoquée par la présence d'un courant accidentel aditionnel : le courant de fuite, qui amplifie dans un sens ou dans l'autre - et selon sa polarité - les effets du courant de corrosion. Attention, les courants de fuite nocifs du bord ou du quai cherchent toujours à rejoindre la mer (leur "terre...") et provoquent une corrosion accélérée du métal conducteur aux points de sortie à la mer ! Les anodes ne sont alors d'aucun secours et seules la détection précoce et la neutralisation rapide de tels courants permettront de vous préserver de leurs coûteuses conséquences !
Le potentiel de corrosion : un indicateur essentiel !
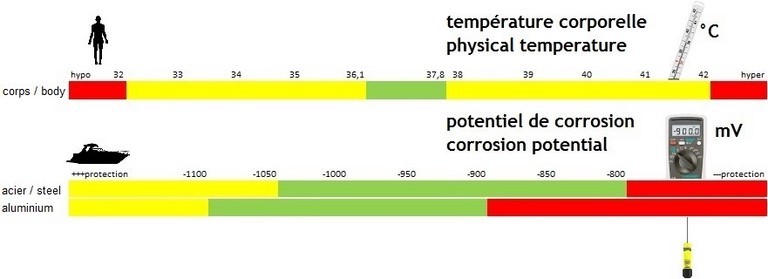
La protection des métaux immergés contre la corrosion est usuellement assurée conjointement par leur couche naturelle d'oxydation et/ou par le système de peinture appliqué, complétée par la protection cathodique disponible (anodes...). Son efficacité dépend de la valeur atteinte par le potentiel de corrosion des métaux protégés, exprimée en (-)mV. A l'image de la température corporelle humaine, son contrôle, à l'aide d'un appareillage approprié, se fait par une simple mesure dont l'interprétation est instantanée : le potentiel de corrosion doit se situer dans l'intervalle de protection (en vert ci-dessus). Sa valeur indique le niveau de protection procuré par les anodes, dont c'est le rôle essentiel, et vous alerte au besoin sur la présence éventuelle de courants de fuite nocifs du bord ou du quai.
Sur et sous-protection : danger !
Au sein d'un même métal une zone anodique se consomme toujours au profit d'une zone cathodique qui se trouve ainsi protégée. Lorsque de telles zones sont volontairement créées au moyen de la mise en contact de différents métaux ou de tout autre système, on parle alors de "protection cathodique".
Les anodes sacrificielles doivent délivrer constamment la quantité de courant de protection nécessaire pour s'opposer au courant de corrosion, et être changées lorsqu'elle devient insuffisante.
Selon leur polarité, les fuites électriques peuvent engendrer des situations de sur- ou de sous- protection cathodique.
La sous-protection cathodique est synonyme d'atteintes de corrosion plus ou moins prononcées, tant sur l'acier (bande n°2) que sur l'aluminium (bande n°3). Elle survient lorsque le potentiel de corrosion est supérieur au seuil maximum de protection requis. La sur-protection cathodique est, quant à elle, susceptible d'entraîner le cloquage et le décollement des peintures sous-marines (bande n°1), voire, des dégâts plus importants. Elle survient lorsque le potentiel de corrosion est inférieur au seuil minimum de protection requis (sens algébrique).
Outre les atteintes éventuelles à la sécurité de la navigation, tous ces phénomènes entraînent des réparations ou des remplacements de pièces pouvant s'avérer extrêmement coûteux.
L'implication du courant alternatif CA : attention au fil de terre !
Le rôle du courant alternatif n'est pas scientifiquement avéré en matière de corrosion des équipements métalliques immergés des navires. En revanche, le fil de terre des installations 230 V du quai est susceptible de véhiculer des courants de fuite continus pouvant affecter de manière importante vos équipements métalliques immergés. Connecté à la masse du bord ainsi qu'exigé par les normes de sécurité en vigueur, cette installation favorise la constitution d'une boucle corrosive. Comme vous ne pourrez jamais préjuger de la qualité des installations du port ou de celles de vos voisins, la prévention passe dès lors par un contrôle régulier du potentiel de corrosion et la pose éventuelle de dispositifs de protection appropriés : isolateurs galvaniques ou transformateurs d'isolement.![]() Inutile de disjoncter pour se mettre à l'abri : le fil de terre by-pass tous les interrupteurs...
Inutile de disjoncter pour se mettre à l'abri : le fil de terre by-pass tous les interrupteurs...
Petit Livre Blanc...

Notas professionnels...

01. La controverse des masses
02. La mise en service des bronzes immergés
03. La corrosion des coques aluminium
04. Les couplages métaux-CFRP
05. L'inaltérabilité des aciers inox
Les anodes
Isolateur ou transformateur ?
Isolateurs galvaniques et transformateurs d'isolement empêchent les courants de fuite de "monter" à bord via la terre du quai. De technologie, fiabilité et efficacités différentes, leur coût varie dans un rapport de 1 à 10.
Le cloquage des peintures
Outre la sur-protection, une cause fréquente de cloquage de la peinture sous-marine d'une coque acier, et plus particulièrement en eaux douces, est la différence de pression osmotique liée à la présence d'impuretés solubles indésirables sous le film de peinture.